Farmacoterapia de la insuficiencia cardíaca y cáncer Estado actual de la evidencia preclínica y clínica
- Dra. Rosanna Guerrero
- febrero 23, 2026
- Consejo Cardio-oncología, Editoriales
- cáncer, consejo cardio-oncología, insuficiencia cardíaca, Rosanna Aguasanta Guerrero
- 0 Comments
La insuficiencia cardíaca (IC) y el cáncer representan dos de las principales causas de morbimortalidad a nivel mundial y, de manera creciente, coexisten en un mismo paciente. El envejecimiento poblacional, la elevada prevalencia de factores de riesgo compartidos —hipertensión arterial, diabetes mellitus, obesidad, tabaquismo, sedentarismo y síndrome metabólico— y los avances terapéuticos en cardiología y oncología han permitido una mayor supervivencia, incrementando la complejidad clínica de esta población. En este escenario, la coexistencia de IC y cáncer se asocia con peor pronóstico, mayor carga de comorbilidades y desafíos relevantes en la toma de decisiones terapéuticas.
En los últimos años ha emergido el concepto de cardio-oncología inversa, que explora la relación bidireccional entre insuficiencia cardíaca y cáncer, así como el posible impacto de la enfermedad cardiovascular crónica y su tratamiento farmacológico sobre la incidencia, progresión y pronóstico de las neoplasias. Los pilares farmacológicos del tratamiento de la IC —betabloqueadores, inhibidores del sistema renina–angiotensina–aldosterona (SRAA), antagonistas del receptor mineralocorticoide (ARM), inhibidores del cotransportador sodio–glucosa tipo 2 (iSGLT2) e inhibidores del receptor de angiotensina–neprilisina (ARNI)— modulan vías fisiopatológicas implicadas tanto en progresión cardiovascular como en carcinogénesis. Aunque la evidencia preclínica demuestra mecanismos biológicos plausibles que sugieren un efecto modulador, la traslación clínica ha sido limitada. Esta revisión de Nabil Sayour y cols en la revista European Heart Journal analiza críticamente la evidencia disponible y discute implicaciones prácticas.
INTRODUCCIÓN
La insuficiencia cardíaca y el cáncer han sido históricamente consideradas entidades independientes. Sin embargo, estudios epidemiológicos han mostrado que los pacientes con insuficiencia cardíaca presentan mayor incidencia de cáncer y mayor mortalidad relacionada con neoplasias, incluso tras ajustar por factores de riesgo compartidos. De manera recíproca, la enfermedad cardiovascular constituye una causa importante de morbimortalidad no oncológica en pacientes con cáncer y puede condicionar la continuidad o intensidad de los tratamientos antineoplásicos.
El desarrollo inicial de la cardio-oncología se centró en cardiotoxicidad por quimioterapia, terapias dirigidas y radioterapia. Posteriormente, el reconocimiento de una relación bidireccional amplió el enfoque hacia la “cardio-oncología inversa”: cómo la insuficiencia cardíaca y su tratamiento podrían influir en cáncer. Este marco conceptual es atractivo porque muchos procesos biológicos relevantes en IC —activación neurohormonal, inflamación crónica, estrés oxidativo, disfunción endotelial e inmunomodulación— también participan en carcinogénesis. No obstante, plausibilidad biológica no equivale a beneficio clínico, y la interpretación requiere rigor metodológico.
RELACIÓN FISIOPATOLÓGICA ENTRE INSUFICIENCIA CARDÍACA Y CÁNCER
La insuficiencia cardíaca es una enfermedad sistémica que trasciende el corazón. La activación crónica del sistema nervioso simpático y del SRAA, junto con la inflamación persistente, promueve un entorno prooxidativo y protrombótico con alteraciones metabólicas. Se han propuesto mecanismos por los cuales esta constelación favorece carcinogénesis: aumento de citocinas (por ejemplo, interleucinas y TNF), remodelado tisular, angiogénesis y cambios en el microambiente que facilitan proliferación y evasión de apoptosis.
Desde una perspectiva inmunológica, la insuficiencia cardíaca se asocia con disfunción de la inmunovigilancia tumoral. Alteraciones en linfocitos T, células natural killer y fenotipos de macrófagos podrían disminuir la capacidad del huésped para identificar y eliminar células premalignas. A esto se suma la comorbilidad frecuente: anemia, enfermedad renal crónica, fragilidad y desnutrición relativa, que pueden agravar disfunción inmune y sesgar resultados observacionales.
Por otra parte, la relación puede ser bidireccional sin causalidad directa. El diagnóstico de IC incrementa el contacto con el sistema de salud y la probabilidad de detección de cáncer. Además, la supervivencia cardiovascular modificada por terapias eficaces puede aumentar el tiempo en riesgo para eventos oncológicos. Estos elementos anticipan la necesidad de incorporar riesgo competitivo y sesgos de detección en cualquier análisis clínico.
MECANISMOS POTENCIALES DE LA FARMACOTERAPIA DE LA IC EN CÁNCER.
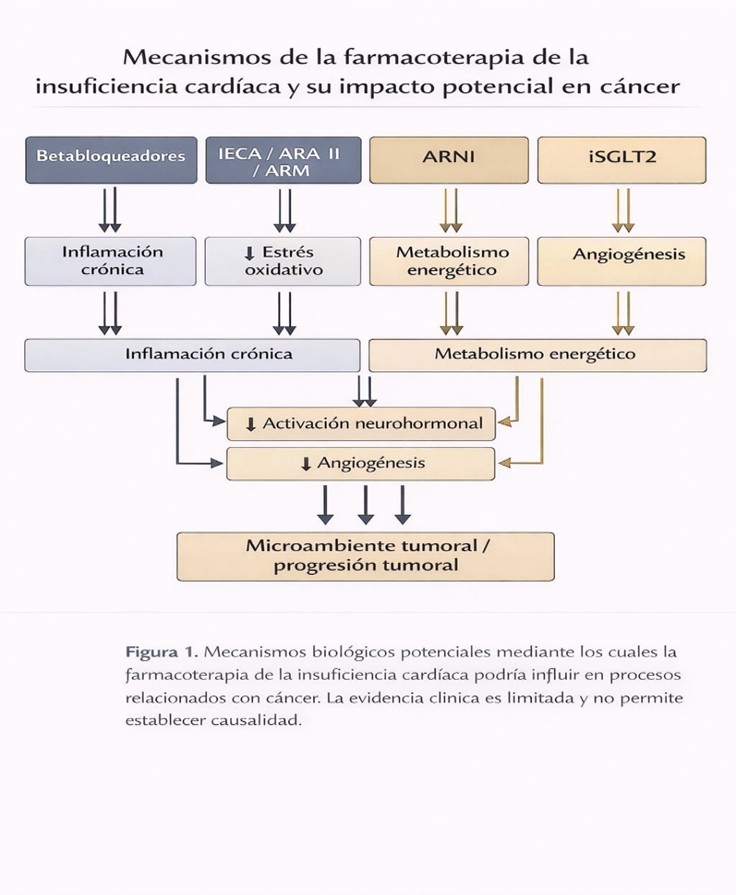
Los fármacos de IC actúan sobre vías biológicas relevantes para cáncer. La señalización beta-adrenérgica se ha vinculado con angiogénesis, invasión y migración celular en modelos experimentales; por tanto, los betabloqueadores podrían reducir señales pro-tumorales. El SRAA, a través de angiotensina II y aldosterona, puede influir en proliferación, fibrosis, estrés oxidativo y respuesta inflamatoria; su inhibición podría modular microambientes tumorales. Los ARM podrían tener efectos sobre fibrosis y remodelado tisular, y los iSGLT2 ejercen efectos metabólicos y antiinflamatorios (reducción de estrés oxidativo, mejoría de eficiencia energética) que podrían impactar, de forma indirecta, procesos relacionados con carcinogénesis. El ARNI introduce además la inhibición de neprilisina, con efectos sobre péptidos natriuréticos y señalización vascular, aunque su traducción oncológica sigue siendo incierta.
La biología tumoral es heterogénea. Un mismo mecanismo puede tener efectos distintos según tipo de tumor, estadio, microambiente y exposición a tratamientos oncológicos. Por ello, el paso de “mecanismo plausible” a “efecto clínico” requiere evidencia prospectiva específica, idealmente con adjudicación de eventos oncológicos, seguimiento suficiente y estrategias analíticas que contemplen riesgo competitivo.
EVIDENCIA CLÍNICA POR CLASES FARMACOLÓGICAS
- La evidencia preclínica favorece un posible efecto antitumoral, especialmente con betabloqueo no selectivo, al reducir señalización catecolaminérgica vinculada con proliferación y metástasis. En humanos, los datos son inconsistentes y dependen del cáncer evaluado, del fármaco y de la indicación. En varios estudios observacionales, la dirección del efecto cambia tras ajustar por comorbilidad, estadio tumoral y uso concomitante de fármacos. Además, existe sesgo por adherencia: pacientes que toman tratamientos crónicos de forma consistente suelen tener mejores desenlaces por conductas saludables y acceso a cuidados, independientemente del fármaco. En insuficiencia cardíaca, su beneficio cardiovascular es incuestionable; por tanto, no existe justificación para iniciar, suspender o cambiar betabloqueo por hipótesis oncológicas no confirmadas.
- Inhibidores del SRAA. En modelos experimentales, IECA y ARA-II muestran señales de modulación de proliferación y angiogénesis. A nivel clínico, la evidencia global es mayoritariamente neutra respecto a incidencia de cáncer. La variabilidad entre estudios se explica por diferencias en duración del seguimiento, definición de cáncer (incidencia vs mortalidad), y mezcla de poblaciones (hipertensión, nefropatía, IC). Un punto práctico es evitar interpretaciones lineales: un resultado “neutro” no descarta efectos en subgrupos específicos, pero tampoco justifica decisiones clínicas sin confirmación prospectiva. En la práctica, se deben indicar por beneficio probado en insuficiencia cardíaca, control hemodinámico y protección renal cuando corresponda.
- Antagonistas del receptor mineralocorticoide. Los ARM reducen remodelado y mortalidad en IC con fracción de eyección reducida. Su evaluación en cáncer es limitada; los estudios disponibles no permiten inferir efectos clínicos robustos sobre incidencia o progresión tumoral. El enfoque clínico debe mantenerse en balance riesgo-beneficio cardiovascular, vigilando hiperpotasemia y deterioro renal, especialmente en pacientes oncológicos con náuseas, deshidratación o nefrotoxicidad por tratamientos antineoplásicos.
- Los iSGLT2 muestran beneficios cardiovasculares y renales consistentes. Los datos sobre cáncer, derivados principalmente de ensayos en diabetes y de programas de IC, no han mostrado señales consistentes de beneficio o daño. Su plausibilidad mecanística se relaciona con mejoras metabólicas, reducción de inflamación y cambios en disponibilidad de sustratos; sin embargo, los desenlaces oncológicos no fueron objetivos primarios. En pacientes con cáncer, el punto clínico es monitorizar estado de volumen, riesgo de cetoacidosis e infecciones genitourinarias, especialmente si hay inmunosupresión o desnutrición.
- Sacubitril/valsartán transformó el manejo de IC con fracción de eyección reducida. Los ensayos pivotales no fueron diseñados para desenlaces oncológicos. Existen consideraciones teóricas sobre neprilisina y péptidos relacionados con proliferación, pero la señal clínica no ha sido consistente. Hasta disponer de evidencia específica, el ARNI debe mantenerse por su beneficio cardiovascular cuando esté indicado y sea tolerado.
INTEGRACIÓN CLÍNICA DE LA EVIDENCIA Y LECTURA PRÁCTICA
En la clínica real, la pregunta clave no es “qué mecanismo es posible”, sino “qué debemos hacer hoy con el paciente”. Con la evidencia actual, la respuesta es prudente: no modificar el tratamiento estándar de insuficiencia cardíaca con fines oncológicos. El riesgo de infratratamiento cardiovascular supera cualquier hipótesis no confirmada. Además, la coexistencia de IC y cáncer exige coordinación multidisciplinaria para sostener terapias de beneficio probado, vigilando interacciones, tolerancia y objetivos del paciente.
Las asociaciones observacionales deben interpretarse bajo el lente del riesgo competitivo. Si una terapia mejora supervivencia cardiovascular, el paciente vive más tiempo y aumenta la probabilidad de que se diagnostique cáncer durante el seguimiento. Sin ajuste adecuado, esto puede parecer un “aumento” de cáncer atribuible al fármaco, cuando en realidad refleja supervivencia. Del mismo modo, pacientes con peor pronóstico pueden morir antes y “protegerse” artificialmente contra el diagnóstico de cáncer, sesgando comparaciones. Estos fenómenos determinan conclusiones clínicas y explican discrepancias entre series y metaanálisis.
En términos prácticos, un abordaje razonable es: (1) confirmar fenotipo de IC y objetivos (reducción de mortalidad, control de congestión, calidad de vida); (2) optimizar GDMT según guías, empezando dosis bajas y titulando con control de presión arterial, función renal y potasio; (3) coordinar con oncología el calendario terapéutico para anticipar períodos de mayor riesgo (neutropenia, deshidratación, nefrotoxicidad); y (4) documentar claramente umbrales de ajuste temporal (hipotensión sintomática, creatinina, potasio), evitando suspensiones prolongadas sin reevaluación. Este marco reduce variabilidad y protege al paciente de decisiones reactivas.
LIMITACIONES Y PERSPECTIVAS FUTURAS
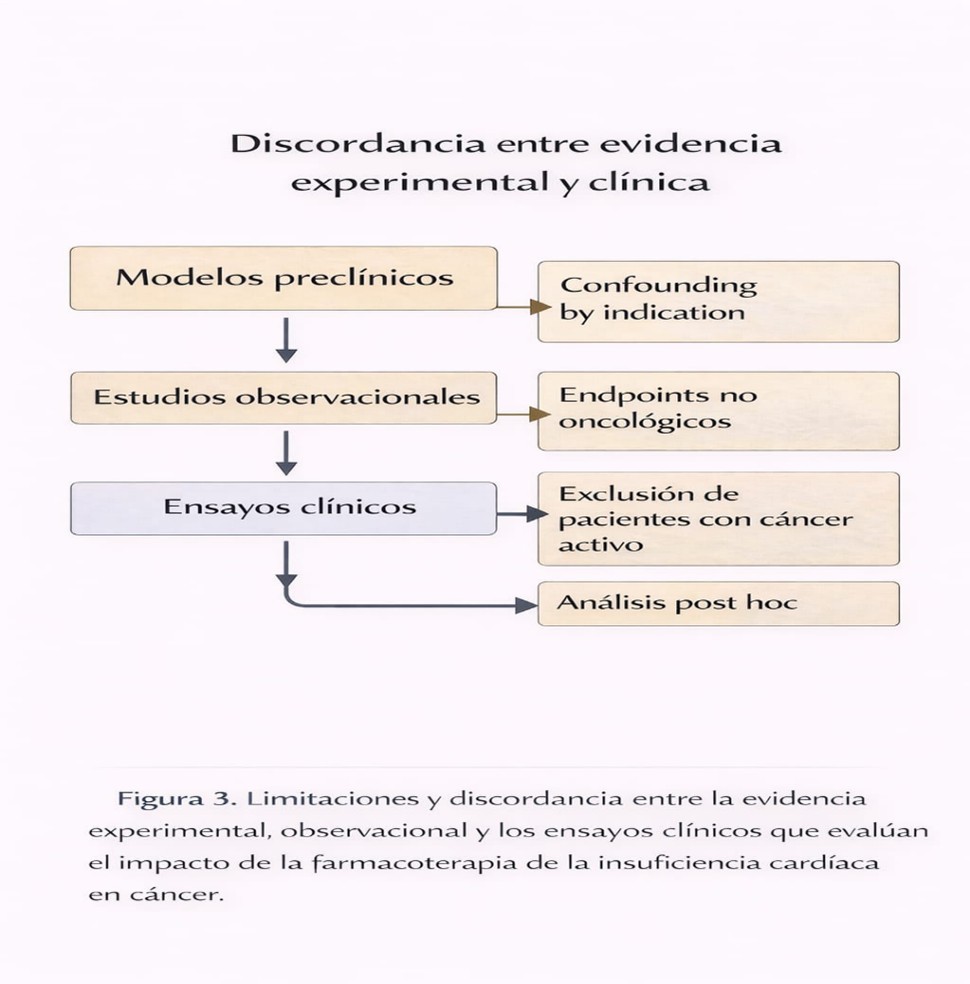
El campo requiere estudios prospectivos diseñados para integrar desenlaces cardiovasculares y oncológicos, con adjudicación sistemática de cáncer, seguimiento prolongado y modelos estadísticos que contemplen riesgo competitivo y sesgos de detección. Además, muchos análisis dependen de registros administrativos, donde la clasificación de cáncer y la temporalidad del diagnóstico pueden ser imprecisas, y donde variables clínicas clave (estadio, tratamientos, recurrencia) no siempre están disponibles. Esto reduce la capacidad de ajustar por gravedad tumoral y por exposición real al fármaco. Por ello, los hallazgos deben considerarse principalmente generadores de hipótesis y no una base para recomendaciones farmacológicas nuevas.
Es importante estudiar subgrupos: pacientes con cáncer previo, supervivientes a largo plazo e individuos con IC que reciben inmunoterapia o terapias dirigidas contemporáneas. Biomarcadores inflamatorios, metabólicos e inmunológicos podrían ayudar a estratificar riesgo y a generar hipótesis testables. Hasta que esa evidencia exista, la recomendación práctica se mantiene: priorizar terapias de IC basadas en guías y sostener colaboración cardio-oncológica.
RECOMENDACIONES OPERATIVAS PARA EL ENTORNO CLÍNICO
En la práctica diaria, la pregunta suele presentarse en forma de dilemas concretos: ¿mantener o no un fármaco durante quimioterapia? ¿qué hacer ante hipotensión o deterioro renal transitorio? ¿cómo priorizar objetivos cuando el cáncer está activo? Un enfoque operativo útil es separar “riesgo agudo” de “beneficio crónico”. En general, los fármacos con beneficio pronóstico (betabloqueadores, SRAA/ARNI, ARM, iSGLT2) deben mantenerse siempre que el paciente esté hemodinámicamente estable, sin hipovolemia ni lesión renal aguda significativa. Cuando existan factores precipitantes reversibles —vómitos, diarrea, mucositis con baja ingesta, sepsis, nefrotoxicidad por quimioterapia— es razonable realizar ajustes temporales, pero con un plan explícito de reintroducción y titulación, evitando suspensiones indefinidas.
Para minimizar eventos, es prudente establecer un “paquete de monitoreo” coordinado con oncología: control de presión arterial (incluyendo ortostatismo), peso, signos de congestión, creatinina y potasio antes de ciclos de mayor riesgo, y reevaluación posterior en 7–14 días si hubo ajustes. En pacientes con terapias oncológicas que prolongan QT o con riesgo de arritmias, debe priorizarse la corrección de electrolitos, revisión de interacciones y un umbral bajo para ECG seriado. Finalmente, el lenguaje al paciente importa: explicar que el tratamiento cardiovascular no se mantiene “por costumbre”, sino porque reduce muerte e ingresos, y que los ajustes se hacen por seguridad, no por temor a hipótesis no demostradas sobre cáncer.
INTEGRACIÓN CLÍNICA DE LA EVIDENCIA Y LECTURA PRÁCTICA PARA EL CARDIÓLOGO
Más allá de la descripción mecanística y de los resultados individuales por clases farmacológicas, resulta fundamental integrar la evidencia disponible desde una perspectiva clínica pragmática. En la práctica real, los pacientes con insuficiencia cardíaca y cáncer constituyen una población compleja, frecuentemente excluida de los ensayos clínicos pivotales, con elevada carga de comorbilidades, fragilidad y polifarmacia.
La ausencia de desenlaces oncológicos preespecificados, el riesgo competitivo y la heterogeneidad de los tipos de cáncer evaluados limitan la capacidad de establecer relaciones causales. Desde el punto de vista clínico, no existe evidencia que justifique iniciar, suspender o modificar la farmacoterapia de la insuficiencia cardíaca con el objetivo de influir en el riesgo de cáncer.
IMPLICACIONES CLÍNICAS
1) No suspender ni retrasar terapias con beneficio pronóstico demostrado en IC por hipótesis oncológicas no confirmadas.
2) Individualizar según tolerancia, presión arterial, función renal y potasio, con reevaluación planificada.
3) Coordinar con oncología para cardioprotección, seguimiento y manejo de interacciones.
4) Comunicar al paciente con claridad y decidir en función de valores y objetivos, especialmente en cáncer avanzado o fragilidad.
CONCLUSIONES
Aunque la farmacoterapia de la insuficiencia cardíaca modula vías biológicas implicadas en carcinogénesis, la evidencia clínica disponible no respalda un beneficio oncológico claro ni justifica cambios en la práctica. La diferencia entre plausibilidad preclínica y evidencia clínica debe guiar una interpretación prudente. El manejo óptimo consiste en aplicar tratamiento estándar de insuficiencia cardíaca basado en guías y sostener una atención multidisciplinaria centrada en el paciente. En síntesis, la mejor ‘estrategia cardio-oncológica’ hoy es sostener el tratamiento óptimo de la insuficiencia cardíaca, anticipar complicaciones de terapias oncológicas y medir resultados con rigor, para que la investigación futura responda con claridad lo que la biología sugiere, pero la clínica aún no confirma.
BIBLIOGRAFÍA
1. Sayour NV, Paál ÁM, Ameri P, Meijers WC, Minotti G, Andreadou I, et al. Heart failure pharmacotherapy and cancer: pathways and pre-clinical/clinical evidence. European Heart Journal. 2024.
2. Aboumsallem JP, Moslehi J, de Boer RA. Reverse cardio-oncology: cancer development in patients with cardiovascular disease. Journal of the American Heart Association. 2020.
3. de Boer RA, Hulot JS, Tocchetti CG, Aboumsallem JP, Ameri P, Anker SD, et al. Common mechanistic pathways in cancer and heart failure. European Journal of Heart Failure. 2020.
4. Bertero E, Canepa M, Maack C, Ameri P. Linking heart failure to cancer. Circulation. 2018.
5. Banke A, Schou M, Videbæk L, Møller JE, Torp-Pedersen C, Gustafsson F, et al. Incidence of cancer in patients with chronic heart failure: a long-term follow-up study. European Journal of Heart Failure. 2016.
6. Hasin T, Gerber Y, Weston SA, Jiang R, Killian JM, Manemann SM, et al. Heart failure after myocardial infarction is associated with increased risk of cancer. Journal of the American College of Cardiology. 2016.
7. Camilli M, Chiabrando JG, Lombardi M, Del Buono MG, Montone RA, Lombardo A, et al. Cancer incidence and mortality in patients diagnosed with heart failure: an updated systematic review and meta-analysis. Cardio-Oncology. 2023.