Guía de Actualización focalizada 2025 de las Guías ESC/EAS 2019 para el manejo de las dislipidemias
- Dr. Fabio Enrique Parada Cabrera
- octubre 7, 2025
- Guías y Consensos
- Carlos Ponte, Dislipemia, estatinas, Fabio Parada, guías, prevención cardiovascular, Sebastián García Zamora
- 0 Comments
Comentario editorial en español en representación de la Sociedad Interamericana de Cardiología (SIAC)
Por Dr Fabio Parada1 Dr. Sebastián García Zamora 2y Dr Carlos Ponte 3
- Miembro del Consejo de Lideres emergentes – Sociedad Interamericana de Cardiología (SIAC)
- Sanatorio Delta, Rosario, Argentina
Director SIAC Academia
Introducción:
La dislipidemia constituye uno de los principales determinantes en el desarrollo y progresión de la enfermedad cardiovascular aterosclerótica (ECVA), que sigue siendo la principal causa de morbimortalidad a nivel mundial. La acumulación progresiva de lipoproteínas que contienen apolipoproteína B (ApoB), especialmente el colesterol de lipoproteínas de baja densidad (LDL-C), en la pared arterial desencadena una cascada de respuestas inflamatorias que promueven la formación y evolución de la placa aterosclerótica. Existe amplia evidencia, tanto epidemiológica como de ensayos clínicos aleatorizados, que respalda la relación causal entre los niveles plasmáticos de LDL-C y el riesgo de ECVA, así como el beneficio clínico consistente de su reducción intensiva. Por lo tanto, la disminución de LDL-C continúa siendo el objetivo central en la prevención y tratamiento de la aterosclerosis.
La Actualización Focalizada 2025 de las Guías ESC/EAS 2019 para el manejo de las dislipidemias surge con el objetivo de incorporar nueva evidencia, incluyendo datos relevantes de ensayos clínicos que evalúan terapias hipolipemiantes emergentes, estrategias de combinación en contextos de alto riesgo, y la importancia de biomarcadores adicionales como la lipoproteína(a).
En este marco, el presente resumen busca sintetizar y contextualizar estas recomendaciones a la práctica clínica en nuestra región, con el propósito de optimizar la estratificación de riesgo, mejorar la adherencia a las metas terapéuticas y favorecer la implementación de un abordaje integral y basado en la mejor evidencia disponible.
Resumen de la guía ESC/EAS 2025:
Estimación del riesgo cardiovascular total e implicaciones para el manejo de la dislipidemia
La aterosclerosis es una patología provocada por la acumulación progresiva de LDL-C y otras lipoproteínas que contienen apolipoproteína-B (ApoB) en la pared arterial, esto que inicia una serie de reacciones inflamatorias que conducen a la formación y avance de la placa aterosclerótica. El LDL-C no sólo constituye un factor de riesgo para la enfermedad cardiovascular aterosclerótica (ECVA), sino que, al igual que otras lipoproteínas que contienen ApoB, es una causa directa de la ECVA; por ende, la reducción de los niveles plasmáticos de LDL-C debe ser el objetivo primordial para prevenir eventos cardiovasculares ateroscleróticos.
El objetivo de estimar el riesgo de una persona de tener un evento cardiovascular aterosclerótico es identificar a los individuos con riesgo elevado que puedan beneficiarse de intervenciones para reducir LDL-C y otras causas modificables de ECVA. Los individuos con mayor riesgo cardiovascular requieren una reducción más intensa del LDL-C para alcanzar el mismo nivel absoluto de riesgo residual bajo tratamiento, en comparación con los individuos de menor riesgo.
La Actualización Focalizada continúa respaldando el concepto señalado en las Guías ESC/EAS 2019: la estimación del riesgo absoluto de una persona de tener un evento cardiovascular agudo debe guiar la intensidad de la reducción de LDL-C.
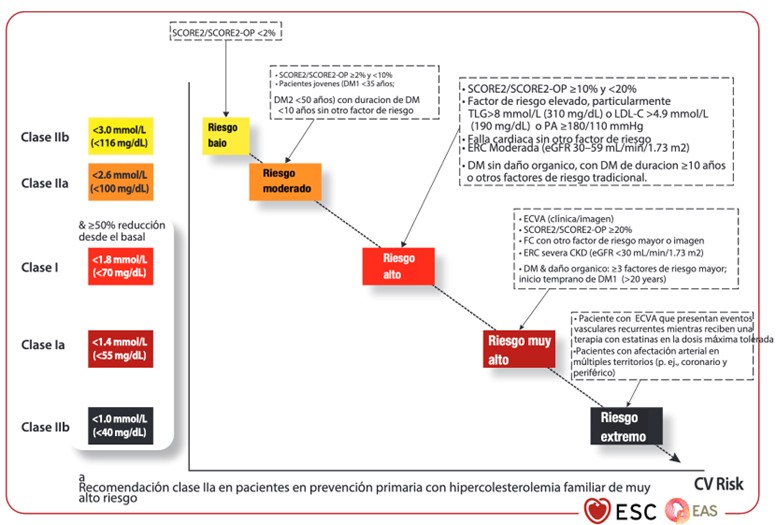
(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
La Actualización Focalizada respalda el uso de escalas de riesgo como SCORE2 y SCORE2-OP (en lugar del algoritmo SCORE) para estimar el riesgo de infarto de miocardio, accidente cerebrovascular isquémico o evento cardiovascular aterosclerótico fatal a 10 años en personas sin enfermedad cardiovascular conocida, con edades entre 40 y 89 años. El algoritmo SCORE evaluaba el riesgo a 10 años de enfermedad cardiovascular fatal en personas de hasta 70 años, los algoritmos SCORE2/SCORE2-OP (disponibles en http://www.heartscore.org) pueden estimar el riesgo a 10 años tanto de eventos cardiovasculares fatales como no fatales también en personas aparentemente sanas de ≥70 años (hasta 89 años).
Es importante recordar que el SCORE2 y SCORE2-OP están calibrados en cuatro grupos de países (riesgo cardiovascular bajo, moderado, alto y muy alto) basados en las tasas nacionales de mortalidad cardiovascular. En esta actualización la Tabla 3 presenta las definiciones actualizadas de riesgo cardiovascular muy alto, alto, moderado y bajo, utilizando SCORE2/SCORE2-OP en lugar del algoritmo SCORE para personas aparentemente sanas (prevención primaria).

(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
El Grupo de Trabajo de la actualización nos recuerda que los modelos poblacionales existentes de riesgo cardiovascular son herramientas relativamente imprecisas para la predicción individual, es razonable prestar atención a características adicionales que se sabe aumentan el riesgo cardiovascular, con el fin de refinar la evaluación de riesgo. Las condiciones clínicas y biomarcadores seleccionados que pueden considerarse modificadores de riesgo. Su presencia puede respaldar la reclasificación de un individuo a una categoría de mayor riesgo que la calculada por el algoritmo SCORE2 o SCORE2-OP, y de este modo guiar las decisiones sobre metas de LDL-C e intervenciones hipolipemiantes.

(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
Aunque no existen ensayos aleatorizados que demuestren que el uso del calcio coronario (CAC) para clasificar el riesgo cardiovascular y guiar el manejo terapéutico mejore los desenlaces cardiovasculares, la consideración del CAC mejora la discriminación y la reclasificación. La consideración del CAC mejora la precisión de la predicción del riesgo cardiovascular mediante el algoritmo SCORE2. Las mediciones de CAC no están indicadas como pruebas de cribado amplias con el propósito de estimación de riesgo cardiovascular; sin embargo, esta Actualización Focalizada incluye una nueva recomendación, la presencia de aterosclerosis subclínica mediante imagen o un puntaje CAC elevado, si se mide, debe considerarse como un modificador de riesgo en individuos con riesgo moderado o cercanos a los umbrales de decisión terapéutica.Se debe considerada que la terapia con estatinas puede llevar a una disminución de la placa rica en lípidos y a un aumento de la calcificación, indicando estabilización de la placa; por lo tanto, el puntaje CAC debe interpretarse con cautela en pacientes tratados con estatinas.
Para los pacientes con diabetes mellitus tipo 2 (DM2) sin ECVA, las Guías ESC 2023 para el manejo de la enfermedad cardiovascular en pacientes con diabetes recomiendan el uso del algoritmo SCORE2-Diabetes para estimar el riesgo cardiovascular a 10 años. Es importante señalar que las metas de tratamiento de LDL-C y la guía terapéutica para cada categoría de riesgo no han cambiado respecto a las Guías ESC/EAS 2019.
La recomendación de iniciar terapia farmacológica de reducción de LDL-C en prevención primaria no se restringe a personas de muy alto riesgo, sino que depende tanto del riesgo cardiovascular estimado como de los niveles basales (no tratados) de LDL-C.
Los algoritmos SCORE2 y SCORE 2-OP fueron derivados de cohortes de participantes sin ECVA clínica que no recibían terapia hipolipemiante. Como resultado, estos algoritmos no deben usarse para estimar el riesgo en personas con ECVA establecida o en personas que actualmente reciben terapia hipolipemiante, ni deben usarse para “reevaluar” el riesgo utilizando mediciones lipídicas obtenidas después de iniciar el tratamiento.
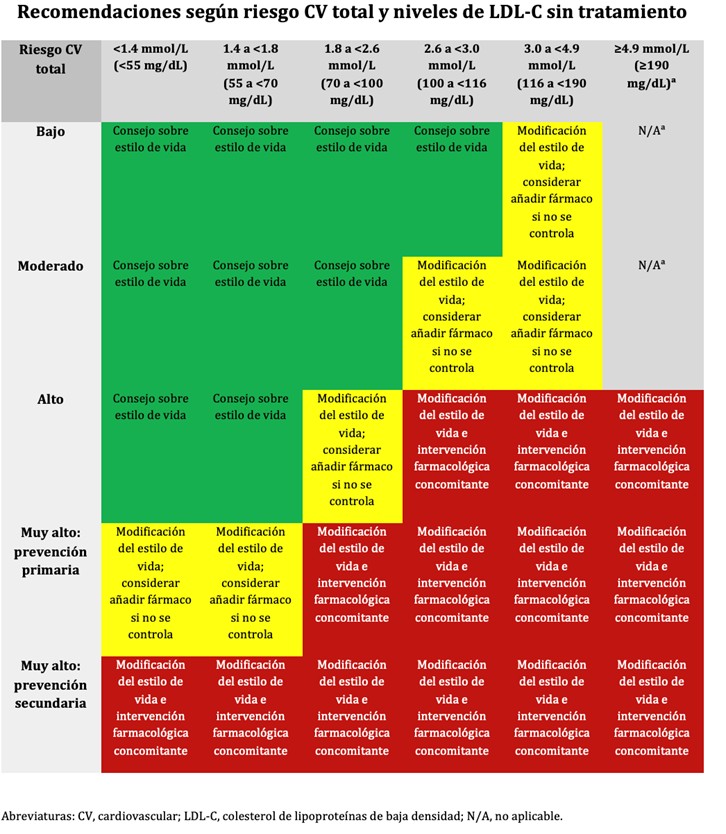
(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
Nuevas terapias para la reducción del colesterol de lipoproteínas de baja densidad (LDL-C)
El ácido bempedoico es una molécula oral de pequeño tamaño que inhibe la síntesis de colesterol al bloquear la acción de la ATP-citrato liasa, una enzima citosólica que actúa aguas arriba de la vía de la 3-hidroxi-3-metilglutaril-coenzima A reductasa. El tratamiento con ácido bempedoico presenta efectos adversos musculares similares al placebo. El ácido bempedoico (disponible en dosis única de 180 mg/día) reduce los niveles de LDL-C aproximadamente en un 23% como monoterapia, en un 18% cuando se administra junto con terapia con estatinas, y en un 38% cuando se administra en combinación a dosis fija con ezetimiba.El estudio CLEAR Outcomes el tratamiento con ácido bempedoico redujo la tasa de MACE, definido como un compuesto de muerte por causas cardiovasculares, infarto de miocardio, accidente cerebrovascular o revascularización coronaria, en un 13% [Hazard risk (HR) 0.87; intervalo de confianza (IC) del 95%, 0.79-0.96; P = 0.004]. No se observó un efecto aparente sobre la mortalidad cardiovascular (HR 1.04; IC 95%, 0.88-1.24).
Debe tenerse en cuenta que existe una considerable variabilidad interindividual en la respuesta de reducción de LDL-C a cualquier fármaco hipolipemiante o combinación, lo que hace necesario monitorizar los efectos del tratamiento después del inicio o la adaptación de cualquier terapia reductora de LDL-C. Tal como se describe en las Guías ESC/EAS 2019, los niveles de LDL-C deben medirse entre 4 y 6 semanas después del inicio o la intensificación de la terapia hipolipemiante.
Inclisiran, una pequeña molécula de ácido ribonucleico interferente (ARNi) que inhibe la síntesis de PCSK9, puede representar un enfoque alternativo a los anticuerpos monoclonales contra PCSK9 (alirocumab y evolocumab). Se ha demostrado en ensayos de fase III que el inclisiran reduce los niveles de LDL-C en aproximadamente un 50%. Actualmente están en curso dos ensayos de desenlaces cardiovasculares con inclisiran [>16 000 pacientes con enfermedad cardiovascular (NCT03705234) y 17 000 pacientes con ASCVD establecida (NCT05030428)], cuyos resultados principales se esperan en 2026 y 2027, respectivamente.
Los pacientes que no pueden tomar estatinas debido a efectos adversos representan un desafío en la práctica clínica. En tales casos, la adición de un agente hipolipemiante no estatínico a una estatina en la dosis máxima tolerada constituye una valiosa opción terapéutica.
Como concepto general, este Grupo de Trabajo recomienda añadir terapias no estatínicas con beneficio cardiovascular demostrado —como la ezetimiba, un anticuerpo monoclonal contra PCSK9 o el ácido bempedoico, en forma individual o combinada— para reducir el LDL-C si no se alcanzan las metas de LDL-C con la dosis máxima tolerada de estatina. La elección debe basarse en la magnitud de la reducción adicional de LDL-C necesaria, la preferencia del paciente, la disponibilidad del tratamiento y el costo.
(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
Combinación de terapias hipolipemiantes durante la hospitalización índice por síndromes coronarios agudos
Los pacientes que experimentan un SCA presentan un riesgo particularmente elevado de recurrencia de eventos cardiovasculares, especialmente durante el primer año tras el alta hospitalaria.
Incluso en un escenario post-SCA ideal, puede tomar hasta 12 semanas para que los pacientes reciban una terapia óptima de reducción de LDL-C siguiendo el enfoque escalonado recomendado en las Guías ESC/EAS 2019. Este período temprano post-SCA corresponde a la fase más vulnerable tras un evento coronario mayor. Los datos observacionales muestran que la terapia intensiva de reducción de lípidos, dirigida por guías, se prescribe con poca frecuencia, con pocos ajustes de dosis después del alta hospitalaria, y que la mayoría de los pacientes no alcanzan sus objetivos.
El estudio IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial) demostró que la adición de ezetimiba a la terapia con estatinas (simvastatina 40 mg) dentro de los <10 días (mediana de 5 días) tras un SCA resultó en una reducción incremental de los niveles de LDL-C y en una disminución modesta pero significativa de los eventos cardiovasculares adversos. Además, datos recientes de los estudios HUYGENS (High-Resolution Assessment of Coronary Plaques in a Global Evolocumab Randomized Study) y PACMAN-AMI (Effects of the PCSK9 Antibody Alirocumab on Coronary Atherosclerosis in Patients With Acute Myocardial Infarction) informaron mejoras en el tamaño y la composición de la placa coronaria en respuesta a una reducción aguda e intensiva de LDL-C en la población vulnerable post-SCA.
Datos recientes del registro SWEDEHEART (Swedish Web-system for Enhancement and Development of Evidence-based care in Heart disease Evaluated According to Recommended Therapies) reportaron el menor riesgo de eventos cardiovasculares en aquellos pacientes que lograron una reducción temprana y sostenida del LDL-C a los niveles recomendados después del infarto de miocardio.
Estos datos respaldan la estrategia terapéutica “cuanto antes, más bajo, mejor” para la reducción del LDL-C en pacientes con SCA. Dado que la magnitud de la reducción de LDL-C en respuesta a las intervenciones farmacológicas es predecible según los niveles basales de LDL-C, es razonable asumir que una proporción significativa de pacientes con SCA no alcanzará su meta únicamente con estatinas de alta intensidad prescritas al alta.
Por lo tanto, y en línea con las Guías ESC 2023 para el manejo de pacientes con SCA, este Grupo de Trabajo propone una estrategia de reducción temprana e intensiva del LDL-C a considerar en todos los pacientes con SCA, con la iniciación inmediata de estatinas y tratamiento combinado con una o más clases de terapias no estatínicas con beneficio cardiovascular comprobado según sea necesario, dependiendo de la terapia hipolipemiante previa al evento. La elección del fármaco para la terapia combinada debe basarse en la magnitud de la reducción adicional de LDL-C requerida. Existen múltiples fármacos y combinaciones con diversas eficacias y velocidades de acción que permiten implementar este enfoque de “golpear temprano y con fuerza”.
Más allá del tratamiento en la fase aguda del SCA, se recomienda controlar los niveles de LDL-C a las 4–6 semanas después de iniciar o intensificar el tratamiento hipolipemiante, y mantener un tratamiento de por vida para reducir el LDL-C a los niveles recomendados.
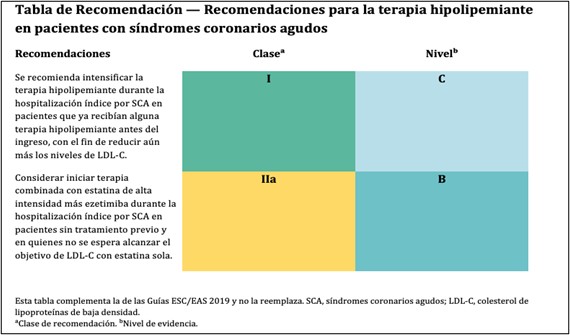
(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
Lipoproteína(a)
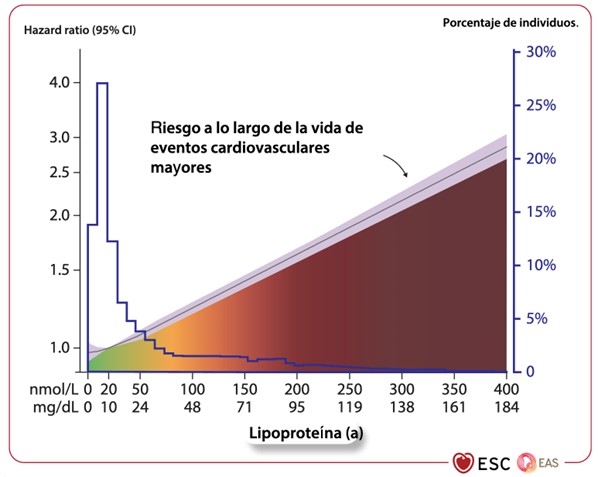
Los estudios epidemiológicos y genéticos respaldan de manera sólida una asociación probablemente causal y continua entre niveles plasmáticos elevados de Lp(a) y mayor riesgo de enfermedad cardiovascular aterosclerótica (ASCVD) y estenosis de la válvula aórtica (AVA). Datos emergentes sugieren que una Lp(a) elevada puede conferir un mayor riesgo de ASCVD y AVA por partícula o por contenido de colesterol que el LDL-C.
El riesgo asociado a una Lp(a) elevada aumenta ligeramente en niveles de 30 mg/dL (62 nmol/L) a 50 mg/dL (105 nmol/L) y se vuelve clínicamente relevante por encima de 50 mg/dL (105 nmol/L), con incrementos progresivos del riesgo cardiovascular a mayores concentraciones.
La concentración de Lp(a) está determinada principalmente por la genética (>90%), más que cualquier otra lipoproteína, y varía según la etnia.La medición de Lp(a) debe considerarse al menos una vez en la vida de cada adulto, ya sea en el primer perfil lipídico o en el siguiente, si ya se han realizado perfiles previos.
El cribado es particularmente relevante en:
- Pacientes jóvenes con HF o ASCVD prematura y sin otros factores de riesgo identificables.
- Personas con antecedentes familiares de ASCVD prematura o Lp(a) elevada.
- Individuos en riesgo moderado o cercanos a umbrales de decisión terapéutica, para mejorar la clasificación de riesgo.
Los niveles de Lp(a) pueden aumentar después de la menopausia, por lo que una segunda medición es razonable, especialmente si los niveles premenopáusicos eran limítrofes.
Aún no se ha demostrado si la reducción de Lp(a) disminuye el riesgo de ASCVD o la progresión de AVA, ni se conoce la magnitud de reducción necesaria para obtener beneficio clínico. En ausencia de terapias específicas para reducir Lp(a), es razonable un manejo temprano de factores de riesgo y una reducción más intensiva de LDL-C, considerando tanto el riesgo cardiovascular absoluto como los niveles de Lp(a).
En siete ensayos clínicos aleatorizados, controlados con placebo y con estatinas, se encontró que las estatinas no tienen efecto sobre las concentraciones de Lp(a). En pacientes con niveles elevados de Lp(a), se debe recomendar firmemente el uso o la continuación de estatinas de alta intensidad si su riesgo cardiovascular es suficientemente alto.
Actualmente, se considera razonable tener en cuenta niveles elevados de Lp(a) >50 mg/dL (≥105 nmol/L) (que afectan al menos al 20% de la población) para refinar la estimación del riesgo CV en todo el espectro de riesgo. Además, este punto de corte debe considerarse como un modificador de riesgo, con potencial para reclasificar la categoría de riesgo CV, particularmente en individuos con riesgo moderado o cercanos a los umbrales de decisión terapéutica.
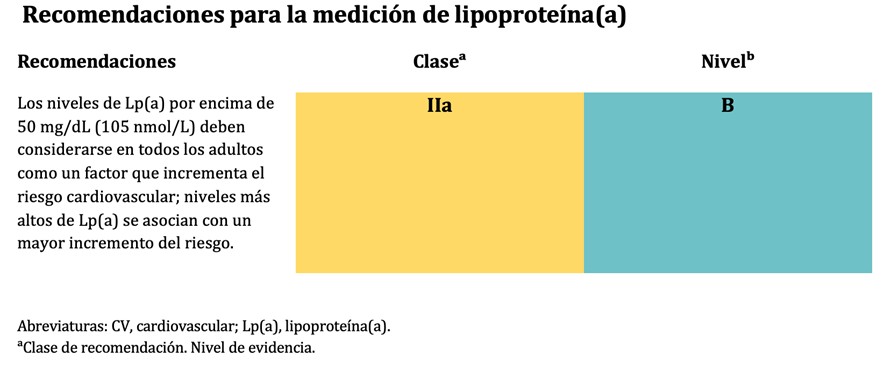
(Adaptado y modificado de 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemia)
Principales Mensajes por Experto SIAC (Dr. Carlos Ponte):
Estratificación del Riesgo Cardiovascular
La actualización 2025 introduce una nueva base para la evaluación del riesgo cardiovascular utilizando las herramientas SCORE2 y SCORE2-OP. Estas permiten estimar el riesgo combinado (eventos fatales y no fatales) a diez años, diferenciando entre el grupo de 40 a 69 años y el de 70 a 89 años, reemplazando así el sistema SCORE clásico que se centraba únicamente en la mortalidad. Además, se incorporan modificadores y criterios de reclasificación, integrando marcadores clínicos y subclínicos tales como historia familiar, inflamación crónica, etnia, calcio coronario y parámetros como IMC y síndrome metabólico. Esto permite afinar la categorización en casos de riesgo intermedio o incierto, mejorando la precisión en la prevención primaria y facilitando decisiones de tratamiento más tempranas en pacientes cuyo riesgo podría ser subestimado por las tablas tradicionales.
Objetivos Lipídicos y Umbrales Terapéuticos
Los objetivos de LDL-C se mantienen en esta edición: para pacientes de muy alto riesgo se establece <55 mg/dL con una reducción ≥50%; para alto riesgo, <70 mg/dL y reducción ≥50%; moderado, <100 mg/dL; y bajo riesgo, <116 mg/dL. Se introduce el concepto de riesgo extremo y la meta para estos pacientes sería < 40 mg/dl
La novedad de 2025 es la definición de umbrales precisos para iniciar farmacoterapia en prevención primaria, vinculados tanto al riesgo estimado como a los niveles basales de LDL-C. Este cambio busca reducir la inercia terapéutica y acelerar las decisiones clínicas, orientando a iniciar tratamiento farmacológico en sujetos de riesgo elevado sin necesidad de esperar deterioro o eventos adversos.
Terapias y Secuencias de Tratamiento. Mientras mas bajo y mientras mas rápido mejor
La estrategia de tratamiento ahora enfatiza la combinación precoz de estatinas de alta intensidad con ezetimiba e, incluso, con inhibidores de PCSK9 desde el inicio en pacientes que requieren reducciones significativas de LDL o se encuentran en escenarios de alto o muy alto riesgo, especialmente tras eventos agudos coronarios. Se incorporan nuevas opciones terapéuticas: ácido bempedoico como alternativa o complemento en casos de intolerancia a estatinas o control insuficiente; inclisirán (ARNi PCSK9, dos dosis al año) que simplifica el seguimiento y la adherencia; y evinacumab (anti-ANGPTL3) para hipercolesterolemia familiar refractaria. Esta ampliación del arsenal terapéutico permite personalizar la intervención, facilitar el logro de metas con menos visitas y mejorar la adherencia, especialmente en casos de LDL difícil de controlar.
Lipoproteína(a) y Triglicéridos
La medición de Lp(a) se recomienda al menos una vez en la vida, reconociéndola como factor causal y herramienta para reclasificar riesgo y ajustar la intensidad del tratamiento. Para la hipertrigliceridemia, se incorpora el uso de icosapento de etilo en pacientes de alto riesgo con triglicéridos elevados pese a tratamiento con estatinas, dada la evidencia de beneficio cardiovascular. Muy importante es la reiteración que los nutracéuticos genéricos y omega-3 convencionales no se recomiendan por falta de evidencia consistente. Estos cambios apuntan a identificar el riesgo residual asociado a Lp(a) y triglicéridos y a dirigir el tratamiento para reducir eventos más allá del control de LDL.
Poblaciones Especiales y Escenarios Clínicos
En el contexto post-SCA, se recomienda la intensificación inmediata del tratamiento combinando fármacos para alcanzar el objetivo <55 mg/dL durante la hospitalización o en las primeras semanas. Además, se ofrecen recomendaciones específicas para poblaciones con condiciones particulares como pacientes que son VIH seropositivos , pacientes oncológicos (cardio-oncología), inflamación crónica, insuficiencia renal crónica, EPOC y diabetes, priorizando la selección y seguridad de los fármacos. Estas matrices prácticas ayudan a reducir la variabilidad y los errores en el manejo de pacientes con comorbilidades frecuentes.
Implementación, Seguimiento y Práctica Clínica
La guía 2025 presenta algoritmos más operativos, con vías rápidas de decisión basadas en el riesgo y la distancia al objetivo de LDL, promoviendo el enfoque de “tratamiento para la meta” y la escalada temprana. Se hace énfasis en esquemas simplificados y de baja carga, como inclisirán, y en la monitorización digital/estructurada para mantener el control a largo plazo. El mensaje central es que los objetivos de LDL no cambian, pero los procesos para estratificar, iniciar, combinar y sostener el tratamiento son ahora más ágiles, personalizados y pragmáticos.
Recomendaciones para la Práctica y Docencia
Se recomienda incorporar de inmediato las herramientas SCORE2/SCORE2-OP, medir Lp(a) al menos una vez y adoptar secuencias combinadas tempranas tras un SCA. En el ámbito educativo, es fundamental destacar que los objetivos de LDL se mantienen, pero la actualización 2025 facilita su logro con más y mejores opciones terapéuticas.
Conflicto de interés: Los autores declaran que no existe ningún conflicto de interés relacionado con la elaboración del presente editorial.
Derechos de autor: El presente editorial constituye una traducción y síntesis del documento original con fines exclusivamente académicos y de divulgación para la comunidad médica hispanohablante. No pretende sustituir la lectura ni la consulta del texto completo en inglés.
Todos los derechos de autor del documento original corresponden a la European Society of Cardiology (ESC) y a la European Atherosclerosis Society (EAS). El texto íntegro, incluyendo tablas, figuras e imágenes, está disponible en las publicaciones oficiales de dichas sociedades.
La presente adaptación se realiza con el único propósito de facilitar la comprensión y aplicación clínica en nuestra región, reconociendo plenamente la autoría y propiedad intelectual de las entidades mencionadas.
Referencia original:
François Mach, Konstantinos C Koskinas, Jeanine E Roeters van Lennep, Lale Tokgözoğlu, Lina Badimon, Colin Baigent, Marianne Benn, Christoph J Binder, Alberico L Catapano, Guy G De Backer, Victoria Delgado, Natalia Fabin, Brian A Ference, Ian M Graham, Ulf Landmesser, Ulrich Laufs, Borislava Mihaylova, Børge Grønne Nordestgaard, Dimitrios J Richter, Marc S Sabatine, ESC/EAS Scientific Document Group. 2025 Focused Update of the 2019 ESC/EAS Guidelines for the management of dyslipidaemias: Developed by the task force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and the European Atherosclerosis Society (EAS). European Heart Journal, 2025; ehaf190. https://doi.org/10.1093/eurheartj/ehaf190