Implante de cardiodesfibrilador para la prevención primaria de muerte súbita cardíaca en cardiomiopatía no isquémica: una mirada sobre la fracción de eyección, la fibrosis en resonancia magnética cardíaca y la genética
- Dr. Daniel Miranda
- abril 22, 2026
- Consejo Cardiomiopatías y Enfermedades del Pericardio, Editoriales
- cardiodesfibrilador, Consejo Miocardiopatías y enfermedades del pericardio, insuficiencia cardíaca, muerte súbita
- 0 Comments
La cardiomiopatía no isquémica (CMNI) constituye un grupo heterogéneo de pacientes en quienes la estratificación del riesgo arrítmico continúa siendo un desafío clínico relevante. En este fenotipo, los modos de muerte se distribuyen fundamentalmente entre la progresión de la insuficiencia cardíaca y la muerte súbita de origen arrítmico, ambas determinantes pronósticas mayores. Este riesgo ha motivado la implantación profiláctica de cardiodesfibriladores implantables (CDI) como estrategia de prevención primaria.
La indicación de CDI en prevención primaria en la CMNI ha transitado un camino complejo en la última década. Tras el impacto del estudio DANISH, la noción de que la fracción de eyección del ventrículo izquierdo (FEVI) ≤35% constituye un criterio suficiente y universal para implantar un CDI comenzó a erosionarse. Desde entonces, el debate no ha sido si el CDI funciona, sino en quiénes aporta beneficio real y medible.
El paradigma clásico —basado casi exclusivamente en la FEVI— resulta hoy insuficiente. La FEVI es un marcador de disfunción global, pero no necesariamente un reflejo directo del sustrato arrítmico. En la CMNI, el riesgo de muerte súbita cardíaca (MSC) depende de la interacción entre remodelado estructural, fibrosis miocárdica, inestabilidad eléctrica y, en muchos casos, predisposición genética. La consecuencia clínica es clara: dos pacientes con la misma FEVI pueden tener perfiles de riesgo radicalmente distintos.
Diversos estudios han demostrado que la presencia de fibrosis miocárdica se asocia de manera robusta con eventos arrítmicos ventriculares, independientemente del grado de disfunción sistólica. Este hallazgo redefine el paradigma tradicional al evidenciar que pacientes con FEVI moderadamente deprimida —o incluso preservada— pueden presentar riesgo arrítmico elevado.
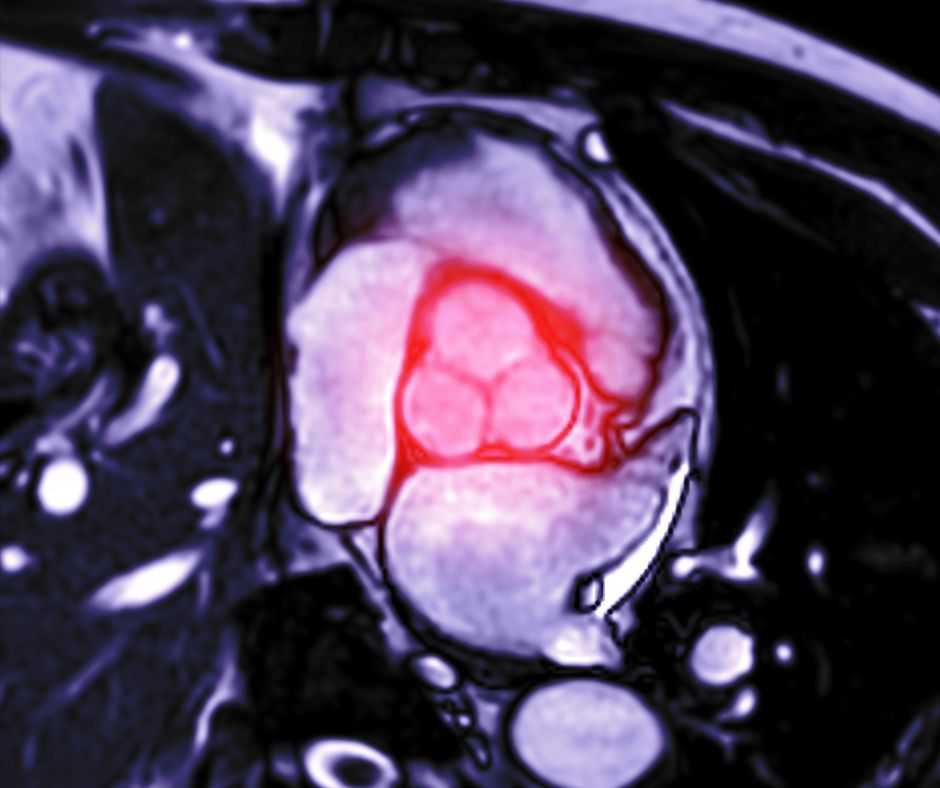
En este contexto, la resonancia magnética cardíaca (RMC) con realce tardío de gadolinio (LGE, por sus siglas en inglés: late gadolinium enhancement) ha emergido como herramienta central en la estratificación arrítmica. La presencia de fibrosis —particularmente en patrón mesocárdico o subepicárdico— se asocia consistentemente con mayor incidencia de arritmias ventriculares y terapias apropiadas del CDI. Más aún, no sólo la presencia sino la extensión y localización de la fibrosis modifican el riesgo. Registros contemporáneos como DERIVATE han demostrado que la distribución segmentaria del LGE mejora la reclasificación del riesgo frente al modelo basado únicamente en FEVI, identificando subgrupos con riesgo arrítmico sustancial aun con FEVI intermedia.
Sin embargo, la búsqueda de un “umbral” absoluto de fibrosis que determine por sí mismo la indicación de CDI debe abordarse con prudencia. La evidencia actual no respalda un punto de corte universal, en parte por variabilidad metodológica en la cuantificación del LGE y en parte porque el riesgo parece comportarse como un gradiente continuo. Estudios recientes sugieren que incluso cargas relativamente bajas de fibrosis pueden asociarse a mayor riesgo arrítmico, mientras que extensiones mayores refuerzan la indicación en pacientes limítrofes. Así, la fibrosis no debe entenderse como criterio binario, sino como elemento integrador dentro de un modelo multiparamétrico.
El registro internacional DERIVATE‑NICM consolidó este concepto al demostrar que la presencia de realce tardío mesocárdico y, especialmente, su distribución y localización segmentaria constituyen predictores independientes de eventos arrítmicos mayores, aportando valor incremental en la reclasificación del riesgo frente al umbral tradicional de FEVI <35%.
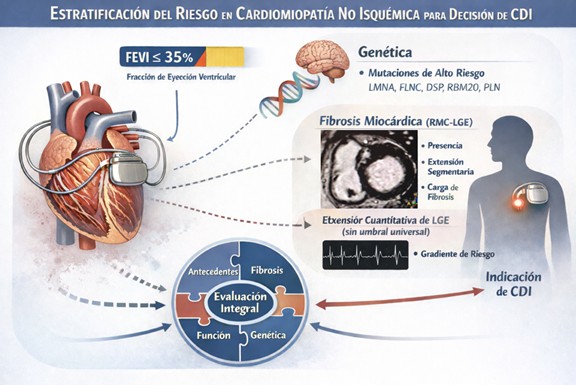
A esta transición conceptual se suma el componente genético. Las guías europeas más recientes de cardiomiopatías enfatizan la evaluación familiar y el estudio genético como parte integral del abordaje de la CMNI. Variantes patogénicas en genes como LMNA, FLNC, DSP, RBM20 o PLN se asocian con fenotipos particularmente arrítmicos, con riesgo desproporcionado de MSC incluso en fases tempranas de la enfermedad y con disfunción ventricular leve o moderada. En estos contextos, el genotipo puede inclinar la balanza hacia una indicación más precoz de CDI, aún cuando la FEVI no cumpla los criterios tradicionales. La genética no reemplaza la imagen; la complementa y, en algunos casos, la anticipa.
De este modo, la prevención primaria en la CMNI se desplaza desde un modelo simplificado —FEVI como único determinante— hacia una estratificación integrada que combina función ventricular, caracterización tisular por RMC, antecedentes familiares, historia arrítmica y perfil genético. Este enfoque no sólo es más fisiopatológicamente coherente, sino también más alineado con el concepto contemporáneo de medicina de precisión.
El desafío clínico actual no radica en abandonar la FEVI, sino en contextualizarla. La FEVI sigue siendo un marcador pronóstico robusto, pero ya no puede operar en aislamiento. La incorporación sistemática de la RMC y, cuando esté indicado, del estudio genético, permite refinar la selección de candidatos a CDI, evitando tanto la sobreindicación como la omisión en pacientes de alto riesgo oculto.
En síntesis, la evidencia acumulada redefine el escenario de la CMNI: el CDI en prevención primaria debe fundamentarse en una evaluación estructural y biológica integral del paciente. La transición del “umbral de FEVI” hacia la caracterización tisular y genética no es una moda conceptual, sino una evolución sustentada en datos. El futuro inmediato no será dicotómico, sino estratificado; no simplista, sino individualizado. Y en esa transición, la RMC y la genética dejan de ser herramientas complementarias para convertirse en pilares de decisión clínica fundamentada.
Bibliografía
- Guaricci AI, Masci PG, Muscogiuri G, Guglielmo M, Baggiano A, Fusini L, et al. Cardiac magnetic resonance for prophylactic implantable-cardioverter defibrillator therapy in non-ischaemic dilated cardiomyopathy: an international registry (DERIVATE). 2021;23:1072-1083.
- Zeppenfeld K, Tfelt-Hansen J, de Riva M, Winkel BG, Behr ER, Blom NA, et al. 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Eur Heart J. 2022;43:3997-4126.
- Heidenreich PA, Bozkurt B, Aguilar D, Allen LA, Byun JJ, Colvin MM, et al. 2022 AHA/ACC/HFSA Guideline for the management of heart failure. J Am Coll Cardiol. 2022;79:e263-e421.
- Guaricci AI, Carrabba N, Romano SM, Chiostri M, Fusini L, Baggiano A, et al. Redefining the risk of major arrhythmic events in non-ischaemic cardiomyopathy: insights from the DERIVATE-NICM study. Eur Heart J Cardiovasc Imaging. 2025;26:1609-1619.
Autores:
Dr. Daniel Miranda. Líder Emergente – Sociedad Interamericana de Cardiología
Dr. Carlos Guamán-Valdivieso. Consejo de Miocardiopatías – Sociedad Interamericana de Cardiología