Mecanismos y manejo de la insuficiencia cardíaca en la persona mayor: cuando la edad biológica supera a la cronológica.
- Dr. Henry De Las Salas
- marzo 22, 2026
- Consejo SIACPrevent, Editoriales
- Alex Rivera, cardiogeriatría, consejo SIACPREVENT, geriatría, Henry de las Salas, insuficiencia cardíaca
- 0 Comments
La insuficiencia cardíaca (IC) en la persona mayor no es simplemente IC en un huésped envejecido: es una enfermedad cualitativamente diferente, modulada por mecanismos biológicos del envejecimiento que las guías actuales no abordan y que los ensayos clínicos pivótales han sistemáticamente subrepresentado. Esta tensión conceptual —entre la evidencia disponible y la realidad clínica de los pacientes que vemos a diario— es precisamente el eje central de la Revisión del Estado del Arte publicado en el European Heart Journal por de Boer et al.¹ Para la cardiogeriatría latinoamericana, este documento representa una hoja de ruta clínica y científica de primer orden.
El riesgo acumulado de desarrollar IC a lo largo de la vida alcanza el 24–25%, con un incremento abrupto de la incidencia tras los 70 años.¹ Los autores subrayan —a partir de la cohorte PREVEND con 25 años de seguimiento y 8.558 participantes— que el riesgo de IC con fracción de eyección preservada (ICFEp) es sustancialmente mayor en mujeres (11,5% vs 6,4% en hombres), mientras que la IC con fracción de eyección reducida (ICFEr) predomina en varones (18,1% vs 11,9%).¹ Este dimorfismo fenotípico según sexo no es trivial; determina diferencias en la fisiopatología predominante, en la respuesta al tratamiento y, de manera crítica, en los objetivos terapéuticos que debe priorizar el clínico. Más preocupante aún resulta la evidencia de que las ganancias en supervivencia logradas hasta 2010 se han erosionado progresivamente, en paralelo con el envejecimiento poblacional y el aumento de la prevalencia de diabetes, obesidad y síndrome cardiovascular-renal-metabólico (CRM): en personas mayores de 65 años, el estadio 3/4 del síndrome CRM afecta al 55,3% de los individuos.²
MECANISMOS DEL ENVEJECIMIENTO CARDÍACO: UNA NUEVA DIANA TERAPÉUTICA
El aporte más original —y clínicamente más provocador— de esta revisión reside en su caracterización de los mecanismos moleculares del envejecimiento cardíaco como contribuyentes activos a la patogénesis de la IC. Cuatro ejes fisiopatológicos sobresalen: (i) el deterioro de la autofagia y la proteostasis, con reducción de la actividad proteasomal demostrada en tejido miocárdico humano con miocardiopatía dilatada e hipertrófica, y una supresión aún más profunda de la autofagia en la ICFEp independientemente de las comorbilidades asociadas³; (ii) la disfunción mitocondrial, que en el corazón —órgano con la mayor densidad mitocondrial del organismo— produce un déficit bioenergético que impulsa el metabolismo glucolítico en etapas avanzadas y condiciona diferencias metabólicas mensurables entre ICFEr e ICFEp; (iii) el inflammaging (envejecimiento inflamatorio o inflamación asociada al envejecimiento) y la senescencia celular, con el fenotipo secretor asociado a senescencia (SASP) correlacionando independientemente con la gravedad clínica tanto en ICFEr como en ICFEp⁴; y (iv) la hematopoyesis clonal de potencial indeterminado (HCPI), cuyas mutaciones —presentes en hasta el 40% de las personas mayores de 70 años— confieren un riesgo cardiovascular comparable al de la hipertensión arterial o la diabetes mellitus tipo 2, con un incremento del 25% en el riesgo de IC de nueva aparición para mutaciones en ASXL1, TET2 y JAK2.⁵ Ninguno de estos mecanismos es abordado por la terapia médica recomendada por guías (TMRG) vigente: ése es, precisamente, el vacío que esta revisión pone sobre la mesa.
PERSPECTIVA CRÍTICA: EFICACIA DE LA TMRG Y SUS LÍMITES EN LA PERSONA MAYOR
De Boer et al. presentan una síntesis rigurosa de los metaanálisis de datos individuales de los grandes ensayos clínicos aleatorizados (SOLVD, MERIT-HF, CIBIS, COPERNICUS, PARADIGM-HF, RALES, EMPHASIS-HF, FINEARTS, DAPA-HF, DELIVER, EMPEROR-Reduced, EMPEROR-Preserved). La conclusión es consistente: los cuatro pilares de la terapía medica optima (TMO) —inhibidores del sistema renina angiotensina aldosterona (SRAA), betabloqueadores, antagonistas del receptor mineralocorticoide (ARM) y gliflozinas— mantienen su eficacia en personas mayores, con términos de interacción estadísticamente no significativos para la edad en todos los metaanálisis. Sin embargo, esta afirmación exige matización clínica. Para los betabloqueadores, el hazard ratio para el cuartil de mayor edad (mediana 75 años) fue de 0,89 (IC 95% 0,78–1,02), comparado con 0,66 (IC 95% 0,56–0,77) en el cuartil más joven: la eficacia relativa se atenúa progresivamente con la edad, aunque la reducción de riesgo absoluto puede preservarse por la mayor morbimortalidad basal de esta población.⁶ La hipotensión arterial, la hiperpotasemia y la disfunción renal son barreras reales, no sólo percibidas, y la selección de pacientes en los ensayos —con exclusión sistemática de personas frágiles, multimórbidas e institucionalizadas— limita la extrapolabilidad directa a la práctica clínica habitual en nuestros servicios, sin embargo en la practica, se puede abordar desde el seguimiento precoz.
En el terreno de los dispositivos, los autores adoptan una postura clínicamente pragmática: la terapia de resincronización cardíaca (TRC) está justificada en personas mayores con bloqueo completo de rama izquierda y QRS > 150 ms con independencia de la edad, mientras que la decisión de implantar un desfibrilador automático implantable (DAI) requiere una valoración individualizada en pacientes mayores de 85 años —o mayores de 80 con comorbilidades significativas—, considerando el riesgo competitivo de muerte no cardíaca. El estudio HF-OPT refuerza esta precaución, al demostrar que la optimización de la TMO durante seis meses conduce a mejoría significativa de la fracción de eyección en un porcentaje relevante de pacientes con ICFEr de reciente diagnóstico, antes de cualquier decisión sobre el DAI.⁷ Finalmente, la revisión integra la planificación anticipada de cuidados como componente ineludible del manejo de la IC avanzada en la persona mayor: una dimensión que las guías ESC y ACC/AHA han incorporado, pero que en la práctica latinoamericana permanece estructuralmente subdesarrollada.
IMPLICACIONES PARA LA PRÁCTICA CLÍNICA
- Implementar la TMO completa en la persona mayor con IC, independientemente de la edad cronológica, ajustando dosis según tolerancia hemodinámica y función renal, sin suprimir fármacos con beneficio pronóstico demostrado por el solo hecho de la edad.
- Distinguir edad biológica de edad cronológica al tomar decisiones terapéuticas: la persona mayor con IC presenta un fenotipo de envejecimiento acelerado que hace inapropiada cualquier estrategia terapéutica basada exclusivamente en el número de años, valorar la fragilidad es necesario.
- Incorporar la evaluación de (HCPI) en un futuro como marcador de riesgo emergente en la persona mayor con IC, especialmente en presencia de ICFEp, a medida que la evidencia clínica sobre su utilidad pronóstica y terapéutica madure.
- Individualizar la indicación de DAI en pacientes mayores de 80 años, evaluando el riesgo competitivo de comorbilidades, y optimizar sistemáticamente la TMO durante al menos 3–6 meses antes de decidir el implante.
- Incorporar la planificación anticipada de cuidados paliativos como eje estructural del seguimiento de la persona mayor con IC avanzada, con discusión explícita y documentada sobre objetivos de calidad de vida versus longevidad, y sobre la desactivación del DAI cuando sea pertinente, apoyandose en cardiogeriatrias o equipos de geriatría.
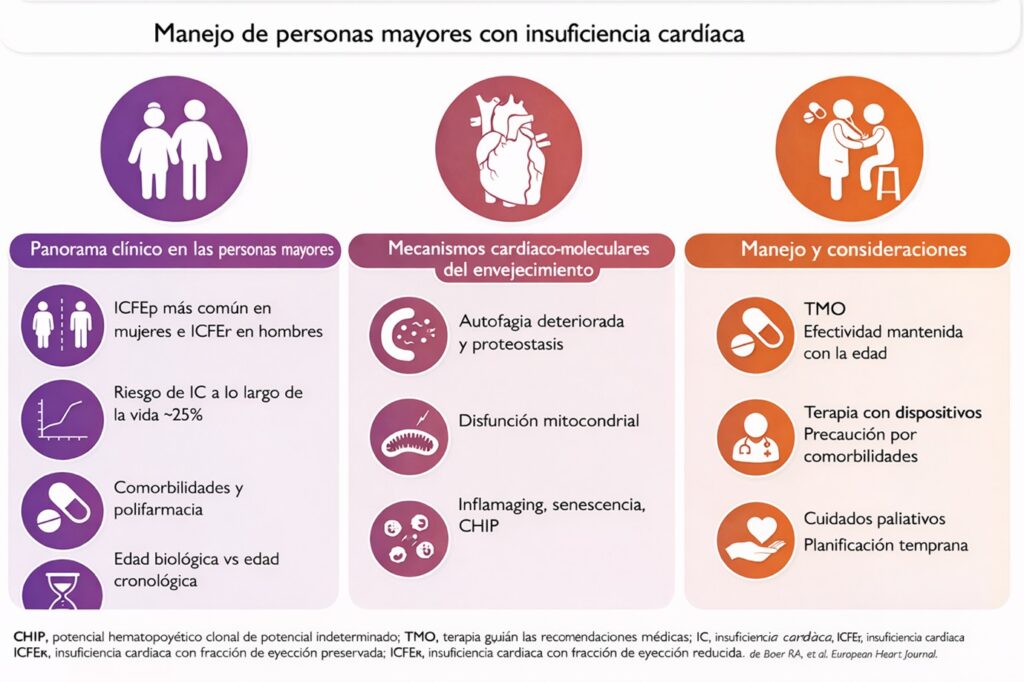
Figura 1. Resumen gráfico: manejo de personas mayores con insuficiencia cardíaca. Adaptado de Eur Heart J. 2026;00,1-13. doi:10.1093/eurheartj/ehag110.
CONCLUSIÓN
La revisión de de Boer et al. establece con claridad que la IC en la persona mayor es un síndrome de envejecimiento acelerado del corazón- un síndrome cardiogeriátrico-, cuya complejidad fisiopatológica desborda los marcos conceptuales actuales de las guías. La TMO sigue siendo el pilar del tratamiento y debe aplicarse con decisión en esta población, superando la inercia terapéutica injustificada. Al mismo tiempo, los mecanismos de envejecimiento miocárdico —autofagia, disfunción mitocondrial, HCPI, senescencia celular— representan dianas terapéuticas emergentes cuya traslación clínica, aunque prometedora, aún carece de evidencia prospectiva de alta calidad en poblaciones humanas. Para el Grupo de Trabajo CardioGeriatría del Consejo SIACPREVENT, este artículo subraya la necesidad urgente de diseñar ensayos clínicos específicamente dirigidos a la persona mayor latinoamericana con IC, una población con una carga de multimorbilidad, fragilidad y acceso diferencial al sistema de salud que exige soluciones propias, no apenas extrapolaciones de cohortes europeas o norteamericanas.
Autores
Dr. Henry De Las Salas. Médico especialista en cardiología geriátrica. Geriatra. Director del Grupo de Trabajo CardioGeriatría del Consejo de Prevención Cardiovascular de la Sociedad Interamericana de Cardiología (SIACPREVENT). Santiago de Chile (Chile).
Dr. Alex Rivera Toquica. Médico especialista en Medicina Interna y Cardiología. Magíster en Epidemiología. Miembro del Grupo de Trabajo CardioGeriatría del Consejo de Prevención Cardiovascular de la Sociedad Interamericana de Cardiología (SIACPREVENT). Codirector del Consejo SIAC Comunidad. CARDIOLOGÍA SAS. Pereira (Colombia).
REFERENCIAS
- de Boer RA, Abdellatif M, Bauersachs J, Roger VL. Heart failure in the elderly: epidemiology, mechanisms, and management. Eur Heart J. 2026. doi:10.1093/eurheartj/ehag110
- Aggarwal R, Ostrominski JW, Vaduganathan M. Prevalence of cardiovascular-kidney-metabolic syndrome stages in US adults, 2011–2020. JAMA. 2024;331:1858–60.
- Hahn VS, Knutsdottir H, Luo X, et al. Myocardial gene expression signatures in human heart failure with preserved ejection fraction. Circulation. 2021;143:120–34.
- Salman O, Zamani P, Zhao L, et al. Prognostic significance and biologic associations of senescence-associated secretory phenotype biomarkers in heart failure. J Am Heart Assoc. 2024;13:e033675.
- Jaiswal S, Libby P. Clonal haematopoiesis: connecting ageing and inflammation in cardiovascular disease. Nat Rev Cardiol. 2020;17:137–44.
- Kotecha D, Manzano L, Krum H, et al. Effect of age and sex on efficacy and tolerability of β blockers in patients with heart failure with reduced ejection fraction: individual patient data meta-analysis. BMJ. 2016;353:i1855.
- Veltmann C, Duncker D, Doering M, et al. Therapy duration and improvement of ventricular function in de novo heart failure: the Heart Failure Optimization study. Eur Heart J. 2024;45:2771–81.